Joka vuosi 17. huhtikuuta on Maailman syöpäpäivä.
01 Maailmanlaajuinen syöpätapausten yleiskatsaus
Viime vuosina ihmisten elämänlaadun ja henkisen paineen jatkuvan kasvun myötä myös kasvainten esiintyvyys on kasvanut vuosi vuodelta.
Pahanlaatuisista kasvaimista (syövistä) on tullut yksi merkittävimmistä kansanterveysongelmista, jotka uhkaavat vakavasti Kiinan väestön terveyttä. Uusimpien tilastotietojen mukaan pahanlaatuisten kasvainten aiheuttama kuolema on 23,91 % kaikista asukkaiden kuolinsyistä, ja pahanlaatuisten kasvainten ilmaantuvuus ja kuolema ovat jatkaneet kasvuaan viimeisten kymmenen vuoden aikana. Syöpä ei kuitenkaan tarkoita "kuolemantuomiota". Maailman terveysjärjestö WHO huomautti selvästi, että niin kauan kuin syöpä havaitaan varhain, 60–90 % siitä voidaan parantaa! Kolmasosa syövistä on ehkäistävissä, kolmannes syövistä on parannettavissa ja kolmasosaa syövistä voidaan hoitaa elämän pidentämiseksi.
02 Mikä on kasvain
Kasvaimella tarkoitetaan uutta organismia, joka muodostuu paikallisten kudossolujen lisääntymisestä erilaisten kasvaimia aiheuttavien tekijöiden vaikutuksesta. Tutkimukset ovat osoittaneet, että kasvainsolujen aineenvaihdunta muuttuu eri tavalla kuin normaaleissa soluissa. Samalla kasvainsolut voivat sopeutua aineenvaihduntaympäristön muutoksiin vaihtamalla glykolyysin ja oksidatiivisen fosforylaation välillä.
03 Yksilöllinen syöpähoito
Yksilöllinen syöpähoito perustuu taudin kohdegeenien diagnoositietoihin ja näyttöön perustuvan lääketieteellisen tutkimuksen tuloksiin. Se tarjoaa perustan potilaille oikean hoitosuunnitelman laatimiseksi, mikä on muodostunut nykyaikaisen lääketieteen kehityksen trendiksi. Kliiniset tutkimukset ovat vahvistaneet, että biomarkkereiden geenimutaatioiden, geenin SNP-tyypityksen, geenien ja niiden proteiinien ilmentymistilan havaitseminen kasvainpotilaiden biologisissa näytteissä lääkkeen tehon ennustamiseksi ja ennusteen arvioimiseksi sekä kliinisen yksilöllisen hoidon ohjaamiseksi voi parantaa tehoa ja vähentää haittavaikutuksia, mikä edistää lääketieteellisten resurssien järkevää käyttöä.
Syövän molekyylitestaus voidaan jakaa kolmeen päätyyppiin: diagnostiseen, perinnölliseen ja terapeuttiseen. Lääketieteellinen testaus on niin kutsutun "terapeuttisen patologian" eli yksilöllisen lääketieteen ydin, ja yhä useampia vasta-aineita ja pienimolekyylisiä estäjiä, jotka voivat kohdistaa kasvainspesifisiin avaingeeneihin ja signalointireitteihin, voidaan soveltaa kasvainten hoitoon.
Kasvainten molekyylikohdennettu hoito kohdistuu kasvainsolujen markkerimolekyyleihin ja puuttuu syöpäsolujen prosessiin. Sen vaikutus kohdistuu pääasiassa kasvainsoluihin, mutta normaaleihin soluihin sillä on vain vähän vaikutusta. Kasvaimen kasvutekijäreseptoreita, signaalitransduktiomolekyylejä, solusyklin proteiineja, apoptoosin säätelijöitä, proteolyyttisiä entsyymejä, verisuonten endoteelikasvutekijöitä jne. voidaan kaikki käyttää kasvainhoidon molekyylikohteina. Kansallisen terveys- ja lääketieteellisen komission 28. joulukuuta 2020 julkaisemat "Syöpälääkkeiden kliinisen käytön hallinnolliset toimenpiteet (koe)" -asiakirjat korostivat selvästi, että selkeiden geenikohteiden omaavien lääkkeiden käytön periaatetta on noudatettava kohdegeenitestauksen jälkeen.
04 Kasvaimeen kohdistuva geneettinen testaus
Kasvaimissa on monenlaisia geneettisiä mutaatioita, ja erityyppisiin geneettisisiin mutaatioihin käytetään erilaisia kohdennettuja lääkkeitä. Potilaat voivat hyötyä vain selvittämällä geenimutaation tyypin ja valitsemalla kohdennetun lääkehoidon oikein. Molekyylitason havaitsemismenetelmiä käytettiin havaitsemaan kasvaimissa yleisesti kohdennettuihin lääkkeisiin liittyvien geenien variaatioita. Analysoimalla geneettisten varianttien vaikutusta lääkkeiden tehoon voimme auttaa lääkäreitä kehittämään sopivimman yksilöllisen hoitosuunnitelman.
05 Ratkaisu
Macro & Micro-Test on kehittänyt sarjan kasvaimen geenien havaitsemiseen tarkoitettuja määrityspakkauksia, jotka tarjoavat kokonaisvaltaisen ratkaisun kasvaimiin kohdennettuun hoitoon.
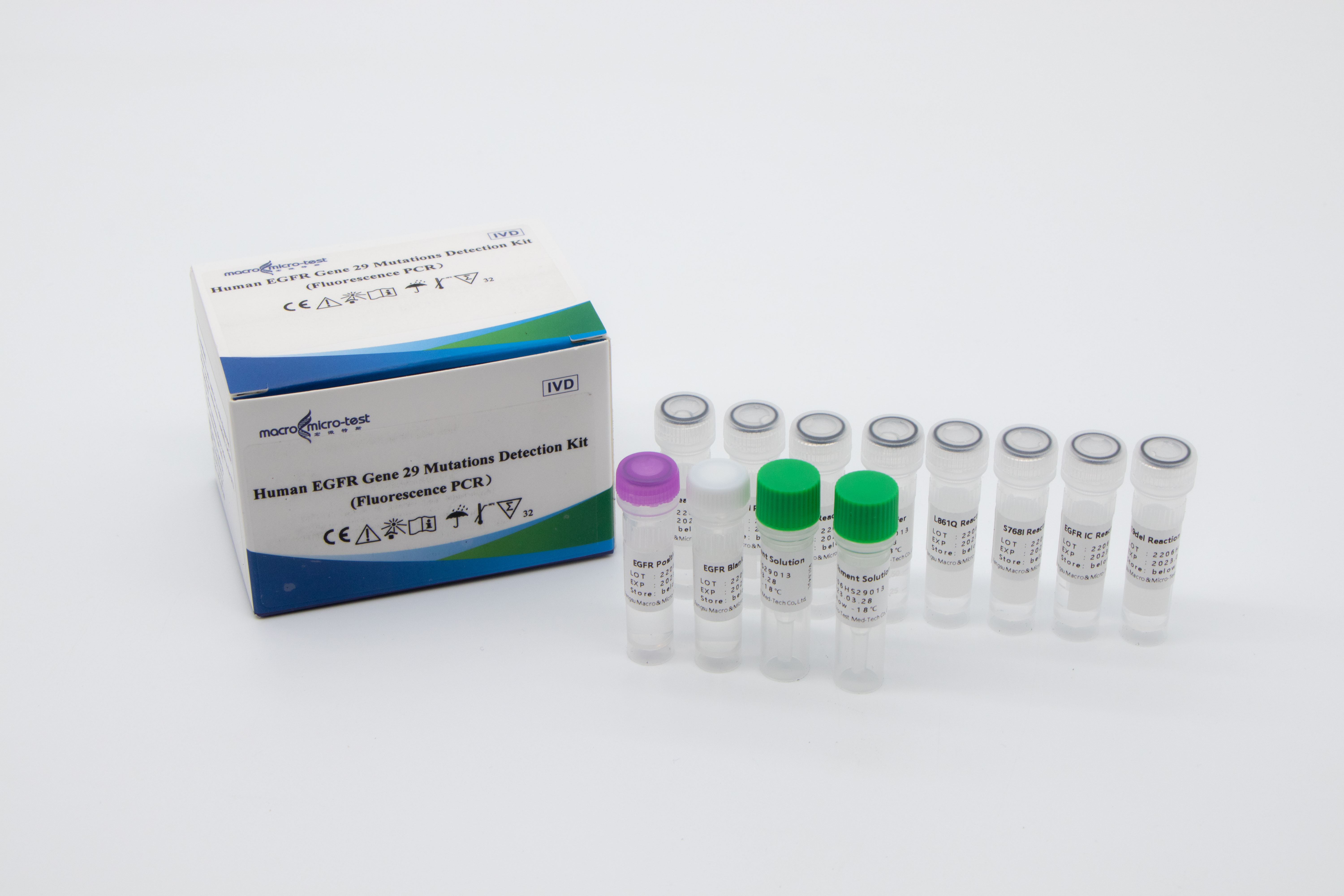
Ihmisen EGFR-geenin 29 mutaatioiden havaitsemispakkaus (Fluoresenssi-PCR)
Tätä testipakkausta käytetään EGFR-geenin eksonien 18–21 yleisten mutaatioiden kvalitatiiviseen havaitsemiseen in vitro ihmisen ei-pienisoluista keuhkosyöpää sairastavien potilaiden näytteissä.
1. Järjestelmä ottaa käyttöön sisäisen vertailulaadunvalvonnan, jolla voidaan kattavasti seurata kokeellista prosessia ja varmistaa kokeen laatu.
2. Korkea herkkyys: Nukleiinihapporeaktioliuoksen havaitseminen voi stabiilisti havaita 1 %:n mutaatioasteen 3 ng/μL villityypin taustalla.
3. Korkea spesifisyys: Ei ristireaktiota villityypin ihmisen genomisen DNA:n ja muiden mutanttityyppien kanssa.
 |  |
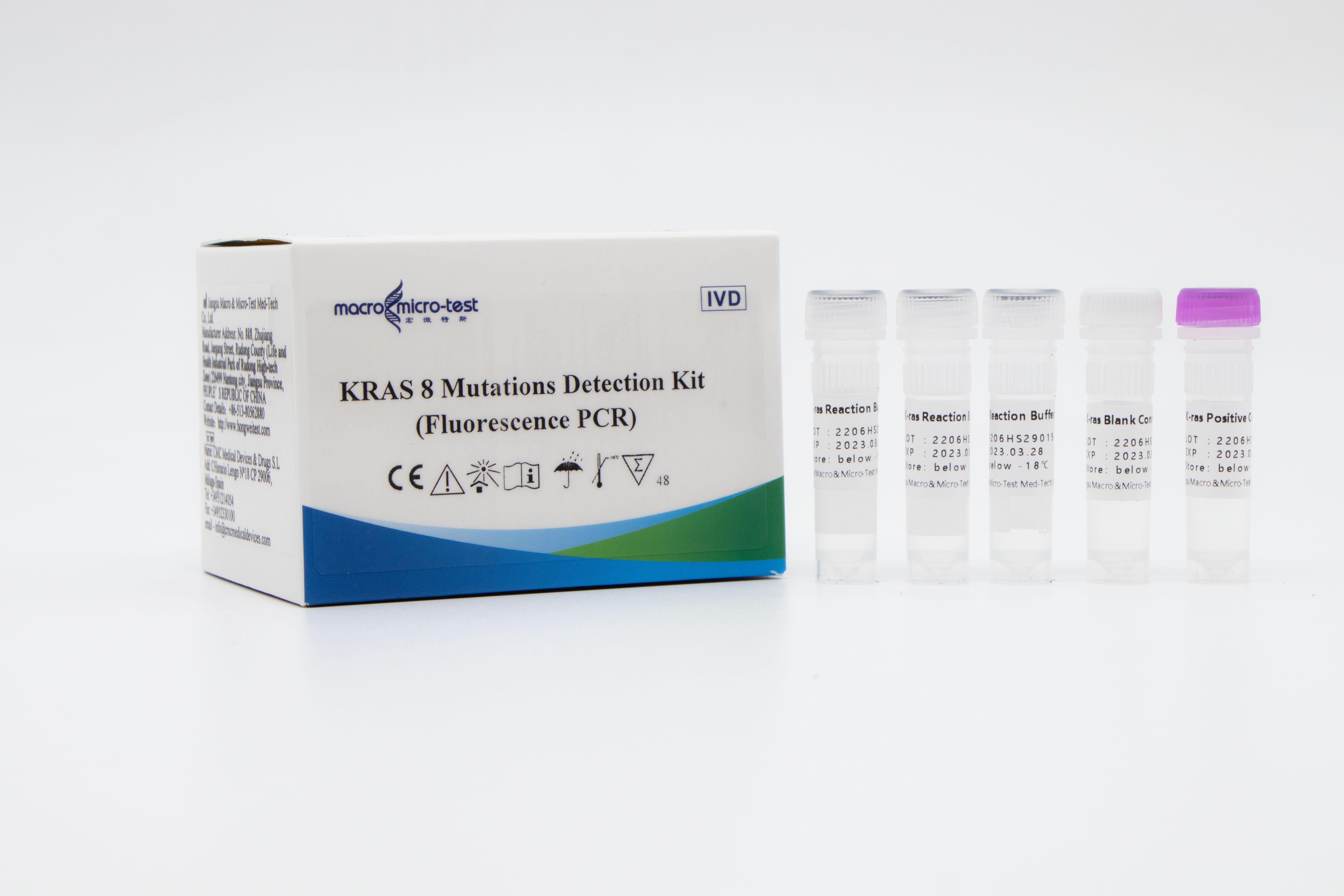
KRAS 8 -mutaatioiden havaitsemispakkaus (fluoresenssi-PCR)
Tämä pakkaus on tarkoitettu K-ras-geenin kodonien 12 ja 13 kahdeksan mutaation kvalitatiiviseen havaitsemiseen in vitro ihmisen parafiiniin upotetuista patologisista leikkeistä uutetussa DNA:ssa.
1. Järjestelmä ottaa käyttöön sisäisen vertailulaadunvalvonnan, jolla voidaan kattavasti seurata kokeellista prosessia ja varmistaa kokeen laatu.
2. Korkea herkkyys: Nukleiinihapporeaktioliuoksen havaitseminen voi stabiilisti havaita 1 %:n mutaatioasteen 3 ng/μL villityypin taustalla.
3. Korkea spesifisyys: Ei ristireaktiota villityypin ihmisen genomisen DNA:n ja muiden mutanttityyppien kanssa.
 |  |
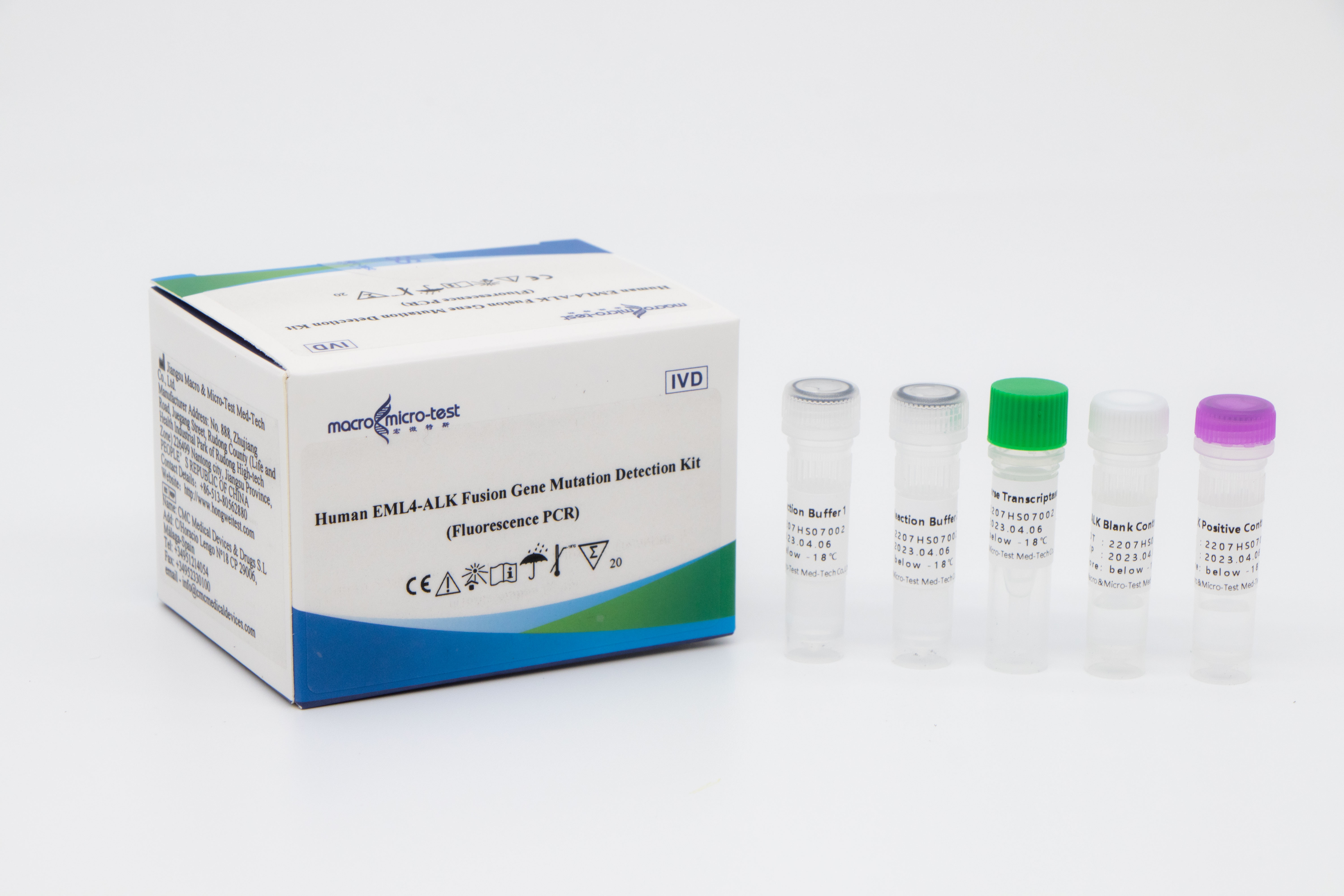
Ihmisen EML4-ALK-fuusiogeenimutaatioiden havaitsemispakkaus (fluoresenssi-PCR)
Tätä testipakkausta käytetään EML4-ALK-fuusiogeenin 12 mutaatiotyypin kvalitatiiviseen havaitsemiseen ihmisen ei-pienisoluista keuhkosyöpää sairastavien potilaiden näytteistä in vitro.
1. Järjestelmä ottaa käyttöön sisäisen vertailulaadunvalvonnan, jolla voidaan kattavasti seurata kokeellista prosessia ja varmistaa kokeen laatu.
2. Korkea herkkyys: Tämä pakkaus pystyy havaitsemaan jopa 20 fuusiomutaatiota.
3. Korkea spesifisyys: Ei ristireaktiota villityypin ihmisen genomisen DNA:n ja muiden mutanttityyppien kanssa.
 |  |
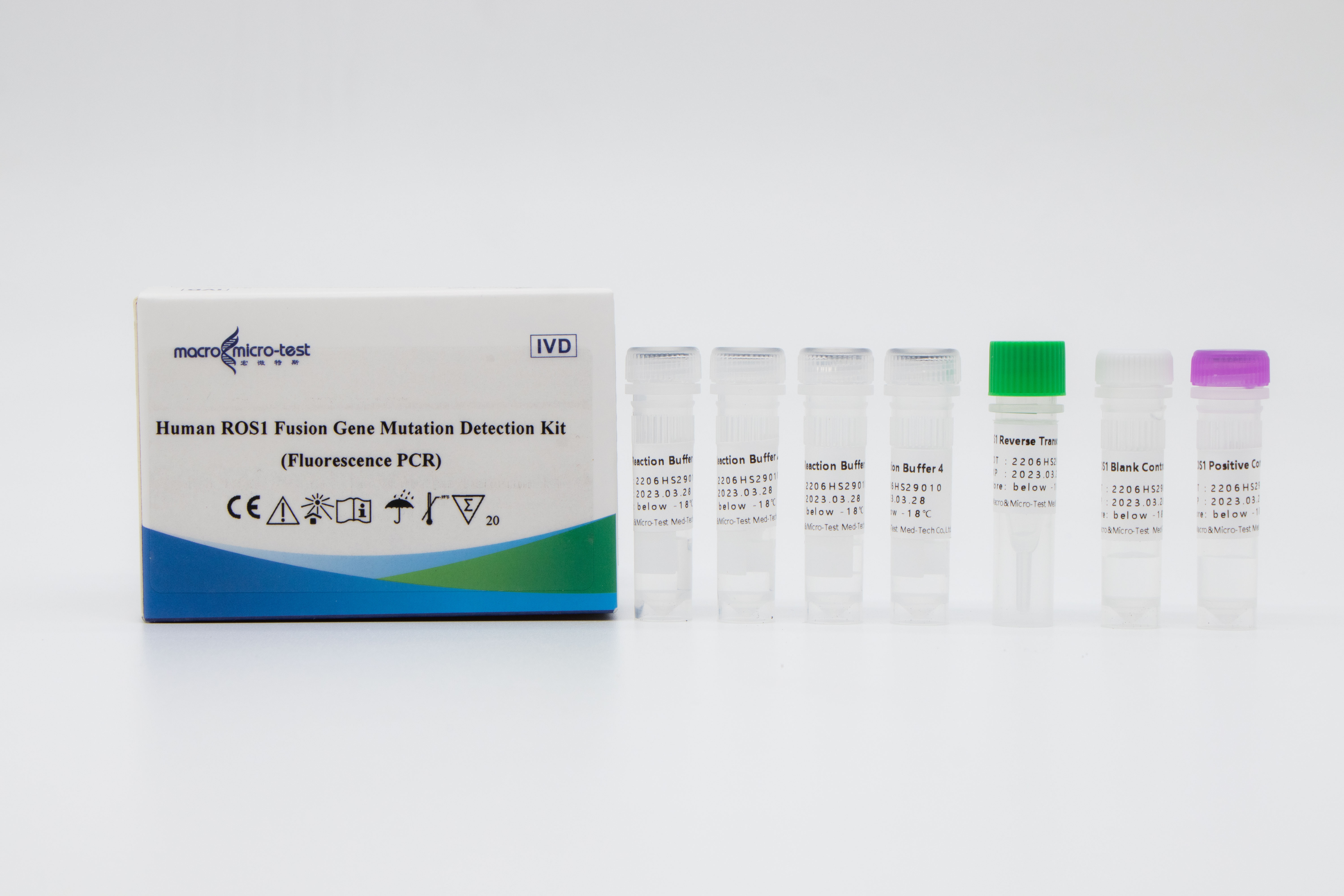
Ihmisen ROS1-fuusiogeenimutaatioiden havaitsemispakkaus (fluoresenssi-PCR)
Tätä testipakkausta käytetään 14 ROS1-fuusiogeenimutaatiotyypin kvalitatiiviseen havaitsemiseen in vitro ihmisen ei-pienisoluisissa keuhkosyöpänäytteissä.
1. Järjestelmä ottaa käyttöön sisäisen vertailulaadunvalvonnan, jolla voidaan kattavasti seurata kokeellista prosessia ja varmistaa kokeen laatu.
2. Korkea herkkyys: Tämä pakkaus pystyy havaitsemaan jopa 20 fuusiomutaatiota.
3. Korkea spesifisyys: Ei ristireaktiota villityypin ihmisen genomisen DNA:n ja muiden mutanttityyppien kanssa.
 |  |
Ihmisen BRAF-geenin V600E-mutaatioiden havaitsemispakkaus (fluoresenssi-PCR)
Tätä testipakkausta käytetään BRAF-geenin V600E-mutaation kvalitatiiviseen havaitsemiseen parafiiniin valetuista ihmisen melanooman, kolorektaalisyövän, kilpirauhassyövän ja keuhkosyövän kudosnäytteistä in vitro.
1. Järjestelmä ottaa käyttöön sisäisen vertailulaadunvalvonnan, jolla voidaan kattavasti seurata kokeellista prosessia ja varmistaa kokeen laatu.
2. Korkea herkkyys: Nukleiinihapporeaktioliuoksen havaitseminen voi stabiilisti havaita 1 %:n mutaatioasteen 3 ng/μL villityypin taustalla.
3. Korkea spesifisyys: Ei ristireaktiota villityypin ihmisen genomisen DNA:n ja muiden mutanttityyppien kanssa.
 |  |
| Luettelonumero | Tuotteen nimi | Tekniset tiedot |
| HWTS-TM012A/B | Ihmisen EGFR-geenin 29 mutaatioiden havaitsemispakkaus (fluoresenssi-PCR) | 16 testiä/pakkaus, 32 testiä/pakkaus |
| HWTS-TM014A/B | KRAS 8 -mutaatioiden havaitsemispakkaus (fluoresenssi-PCR) | 24 testiä/pakkaus, 48 testiä/pakkaus |
| HWTS-TM006A/B | Ihmisen EML4-ALK-fuusiogeenimutaatioiden havaitsemispakkaus (fluoresenssi-PCR) | 20 testiä/pakkaus, 50 testiä/pakkaus |
| HWTS-TM009A/B | Ihmisen ROS1-fuusiogeenimutaatioiden havaitsemispakkaus (fluoresenssi-PCR) | 20 testiä/pakkaus, 50 testiä/pakkaus |
| HWTS-TM007A/B | Ihmisen BRAF-geenin V600E-mutaatioiden havaitsemispakkaus (fluoresenssi-PCR) | 24 testiä/pakkaus, 48 testiä/pakkaus |
| HWTS-GE010A | Ihmisen BCR-ABL-fuusiogeenimutaatioiden havaitsemispakkaus (fluoresenssi-PCR) | 24 testiä/pakkaus |
Julkaisun aika: 17. huhtikuuta 2023
