I. YleiskatsausESMOVuoden 2025 ohjeistus
Elokuussa 2025 ESMO julkaisi virallisesti Early and locally advanced non-small cell lung cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up -ohjeiston, joka julkaistiin johtavassa onkologisessa julkaisussa Annals of Oncology. Tämä on ensimmäinen kattava päivitys vuoden 2017 version jälkeen ja tarjoaa erittäin arvovaltaisen lähdemateriaalin onkologeille maailmanlaajuisesti.

Keuhkosyöpä on maailmanlaajuisesti yleisin ja kuolleisin syöpätyyppi. Joka vuosi todetaan yli 2,2 miljoonaa uutta tapausta ja yli 1,8 miljoonaa kuolemantapausta, mikä tekee keuhkosyövästä johtavan syöpään liittyvän kuolemansyyn sekä miehillä että naisilla. Ei-pienisoluinen keuhkosyöpä (NSCLC) muodostaa noin 80–85 % kaikista keuhkosyöpäpotilaista. Tätä vakavaa tilannetta vasten vuoden 2025 ohjeistuksen julkaiseminen tuo uutta tieteellistä vauhtia kliiniseen käytäntöön, ja biomarkkeritestausstrategioiden päivitys on erityisen tärkeää.
II. Keskeisten ohjepäivitysten tulkinta
2.1 Biomarkkeritestaus: ”Valinnaisesta” ”välttämättömään”
Vuoden 2025 ohjeistus tekee merkittävän strategisen muutoksen biomarkkeritestaukseen. Ohjeistus toteaa nimenomaisesti, että biomarkkeritestaus on välttämätöntä hoitopäätösten tekemiseksi potilailla, joilla on vaiheen IB-III ei-pienisoluinen keuhkosyöpä.
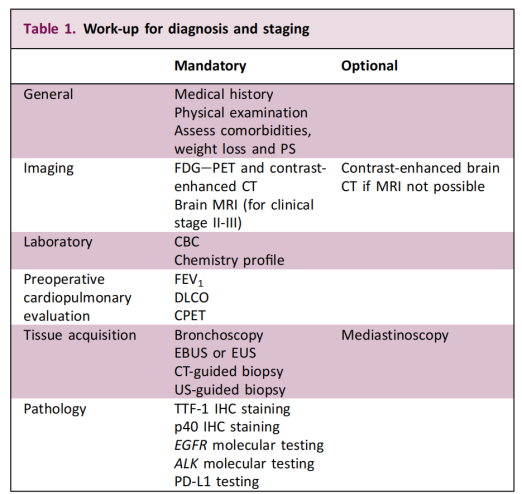
Tämä suositus laajentaa molekyylitestausta aiemmasta keskittymisestä pitkälle edenneen taudin potilaisiin varhaisvaiheen, resektoitaviin tapauksiin. Keskeisenä tavoitteena on tunnistaa ajurigeenimutaatiot ja tarjota tieteellinen perusta yksilölliselle täsmähoidolle. Ohjeistus korostaa myös, että biopsian toteutettavuuden ja diagnostisen lähestymistavan tulisi määrittää moniammatillinen tiimi potilaan ja kasvaimen ominaisuuksien perusteella.
Tarkemman testausstrategian osalta ohjeessa suositellaan selvästi, että geneettinen testaus suoritetaan ennen kirurgista päätöksentekoa ja että sen tulisi kattaa ainakin EGFR ja ALK. Tällä "etukäteisen testauksen" käsitteellä on syvällinen kliininen merkitys varhaisvaiheen NSCLC:n tarkan luokittelun ja yksilöllisen hoidon kannalta – testitulosten ajantasaisuus ja tarkkuus määräävät suoraan myöhemmän adjuvanttihoidon valinnan.
2.2 Lääketieteelliset läpimurrot kuljettaja-onkogeenipositiivisessa varhaisvaiheen ei-pienisoluisessa keuhkosyövässä
Vuoden 2025 ohjeistus yhdistää useista merkittävistä kliinisistä tutkimuksista saatua näyttöä selkeän täsmähoitopolun luomiseksi kuljettaja-onkogeenisesti positiivista varhaisvaiheen ei-pienisoluista keuhkosyöpää sairastaville potilaille.
EGFR-mutaatiopositiiviset potilaat:Merkittävän ADAURA-tutkimuksen perusteella kolmen vuoden ajan leikkauksen jälkeisestä adjuvantista osimertinibistä on tullut maailmanlaajuinen hoitostandardi potilaille, joilla on EGFR-eksonin 19 deleetioita tai eksonin 21 L858R-mutaatioita. ADAURA-tutkimus on kansainvälinen, monikeskustutkimus, satunnaistettu ja kontrolloitu vaiheen III tutkimus, jossa arvioidaan adjuvanttina annetun osimertinibin tehoa ja turvallisuutta potilailla, joilla on täysin resektoitu vaiheen IB-IIIA EGFR-mutatoitunut ei-pienisoluinen keuhkosyöpä. Tutkimus osoitti, että osimertinib paransi merkittävästi sekä tauditonta eloonjäämistä että kokonaiseloonjäämistä lumelääkkeeseen verrattuna, mikä vakiinnutti osimertinibin uudeksi hoitostandardiksi tälle potilasryhmälle. ADAURA-tutkimuksen eksploratiiviset analyysit kuitenkin osoittivat, että noin 36 % hoidon ennenaikaisista lopettamisista johtui haittavaikutuksista ja toiset 31 % potilaan omasta päätöksestä. Tämä havainto korostaa tarkkojen lähtötason mittausten tarvetta ennen hoitoa, jotta voidaan varmistaa, että kohdennettua hoitoa annetaan potilaille, jotka voivat saada siitä pysyvää hyötyä.
ALK-positiiviset potilaat:ALINA-tutkimuksen perusteella alektinibihoito leikkauksen jälkeisenä adjuvanttina kahden vuoden ajan on nyt standardihoito. Vaiheen III satunnaistetun avoimen ALINA-tutkimuksen ensisijaisessa analyysissä alektinibi osoitti merkittävää tauditonta eloonjäämistä parantavaa vaikutusta vaiheen II-IIIA potilailla, riskisuhteen ollessa 0,24. ESMO 2025 -kongressissa esitellyt ALINA-tutkimuksen päivitetyt tiedot osoittivat, että ≥3 vuoden seurannan jälkeen alektinibin tautivapaata eloonjäämistä parantava hyöty pysyi "jatkuvana ja kliinisesti merkittävänä", riskisuhteen ollessa 0,36 vaiheen II-IIIA potilailla. Viimeisin raportoitu neljän vuoden kokonaiselossaoloprosentti oli 98,4 %, neljän vuoden tautivapaa elossaoloprosentti oli 75,5 % ja myös keskushermoston tautivapaa elossaoloprosentti parani, eikä uusia turvallisuussignaaleja ilmennyt. Nämä vankat tiedot vahvistavat entisestään alektinibihoidon standardihoidon merkityksen ALK-positiivisen ei-pienisoluisen keuhkosyövän resektiossa ja korostavat tarkan testauksen arvoa tällaisten potilaiden tunnistamiseksi.
Testausmenetelmän valinta:Vuoden 2025 ESMO-ohjeessa luetellaan nimenomaisestimultipleksiset RT-PCR-paneelimäärityksetRNA-pohjaisen NGS:n, IHC:n ja FISH:n ohella yhtenä suositelluista teknisistä menetelmistä ALK-fuusion havaitsemiseksi. Tämä osoittaa, että ohjeistuksen ydinvaatimus on suorittaa testejä kliinisten päätösten ohjaamiseksi eikä määrätä tietystä testausalustasta. EGFR:n ja ALK:n havaitsemiseen keskittyville RT-PCR-tuotteille tämä joustava testausstrategia tarjoaa vahvan ohjeistukseen perustuvan perustelun niiden kliiniselle käytölle.
III. Tarkkuustestauksen tekniset ratkaisut
Vuoden 2025 ohjeistus siirtää testausta leikkausta edeltävään päätöksentekovaiheeseen, mikä nostaa rimaa määritysmenetelmien tarkkuudelle, herkkyydelle ja saavutettavuudelle. Kaksi alla kuvattua RT-PCR-pohjaista havaitsemistuotetta vastaavat teknisestä näkökulmasta täysin ohjeistuksen vaatimuksia.
3.1 EGFR-mutaatioiden havaitsemispakkaus – parannettu ARMS-teknologia-alusta
YdinteknologiaParannettu ARMS-teknologia mahdollistaa vähäisten mutanttisekvenssien spesifisen monistamisen korkeaa villityypin taustaa vasten
Kolme teknistä suojatoimenpidettä:
-Parannettu ARMS → parantaa mutaatioiden tunnistusta
-Entsymaattinen rikastus → pilkkoo villityypin taustaa ja rikastaa mutanttisekvenssejä
-Lämpötilan esto → estää epäspesifisen vahvistuksen
SuorituskykyHerkkyys1 % mutanttialleelifrekvenssi
Saastumisen torjuntaSisäänrakennettu sisäinen kontrolli + UNG-entsyymi estävät kontaminaation
LäpimenoaikaSuljetun putken toiminta, noin120 minuuttia
Näytteiden yhteensopivuus:Kudos/nestemäinen biopsianäytteet → täyttää "etukäteisen testauksen" vaatimuksen
Kattavuus:45 mutaatiotaEGFR-eksoneissa 18–21, täsmälleen ohjeissa korostettujen alueiden mukaisesti (eksonin 19 deleetiot ja eksonin 21 L858R)
Kliininen käyttöOhjaa suoraan EGFR-TKI-hoitoa
3.2 MMT EML4-ALK -fuusioiden havaitsemispakkaus – RNA-pohjainen fuusioiden havaitsemisratkaisu

-Teknologia-alustaRNA-pohjainen RT-PCR – tarjoaa luonnostaan etuja DNA-pohjaisiin menetelmiin verrattuna fuusioiden havaitsemisessa
-RNA-pohjainen etuHavaitsee suoraan ilmentyneet fuusiotranskriptit, välttäen tehokkaasti vääriä negatiivisia tuloksia
-TutkimusnäyttöAlhaisen ALK-fuusiomäärän omaavissa fuusioissa RT-PCR on huomattavasti luotettavampi kuin DNA-pohjaiset testit.
-HerkkyysHavaitsee fuusiot jopa20 kopiota reaktiota kohden
-Varianttien kattavuusKannet12 yleistä EML4-ALK-fuusiovarianttia(mukaan lukien variantti 1 ~33 %; variantit 3a/3b yhteensä ~29 %)
-Käyttö ja kontaminaationhallintaSuljettu putki, ~120 minuuttia; sisäänrakennetut prosessinsäätimet + UNG-entsyymi estävät virheelliset tulokset
-Instrumenttien yhteensopivuusYhteensopiva useiden yleisten reaaliaikaisten PCR-laitteiden kanssa
-Ohjeiden kohdistusErittäin yhdenmukainen ESMO:n ohjeiden kanssa
IV. Määritysten ja ohjeiden suositusten välinen yhdenmukaisuus
Nämä kaksi havaitsemistuotetta ovat erittäin yhdenmukaisia ESMO 2025 -suosituksen kanssa varhaisen ja paikallisesti levinneen ei-pienisoluisen keuhkosyövän hoidossa seuraavien keskeisten osa-alueiden osalta:
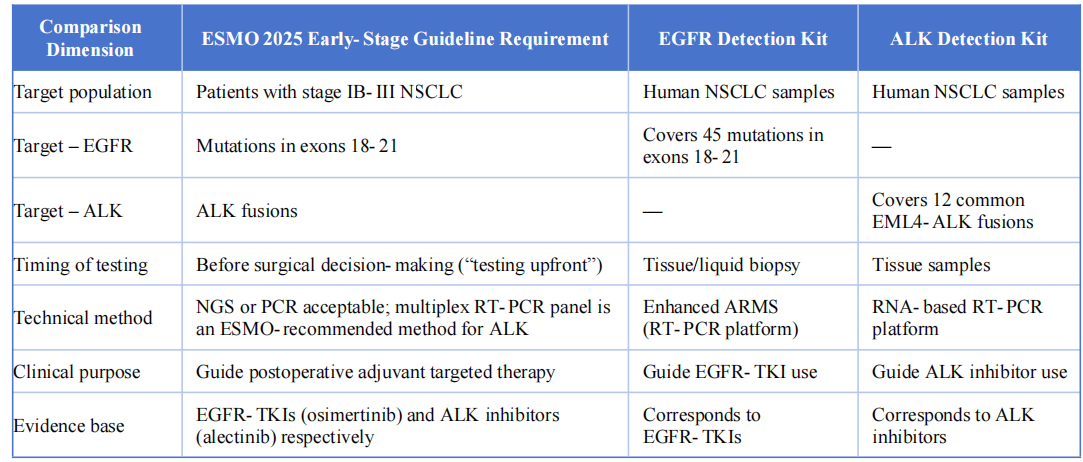
V. Johtopäätös
ESMO 2025 -ohjeistus varhaisvaiheen ei-pienisoluisen keuhkosyövän hoidosta aloittaa uuden aikakauden täsmädiagnostiikassa ja -hoidossa, jonka keskipisteenä on ”etukäteistestaus, tarkka kohdentaminen ja hoidon optimointi.”EGFR-mutaatioiden havaitsemispakkaus ja MMT EML4-ALK-fuusioiden havaitsemispakkaus täyttävät ohjeiden vaatimukset kohteiden, ajoituksen ja tarkkuuden suhteen erillisten teknisten polkujen kautta.”
EGFR-pakkaus käyttää parannettua ARMS-teknologiaa kohdennettujen mutaatioiden havaitsemiseen erittäin herkästi rajoitetuissa näytteissä, tukien sekä kudos- että nestebiopsiaa, jotta "testaus etukäteen" olisi mahdollista.
ALK-testi perustuu RNA-pohjaiseen RT-PCR:ään, mikä tarjoaa etuja DNA-menetelmiin verrattuna fuusioiden havaitsemisessa ja on linjassa ESMO:n suosituksen kanssa ALK-testauksessa käytettävistä multipleksisista RT-PCR-paneeleista.
Yhdessä nämä kaksi tuotetta muodostavat ESMO 2025 -ohjeistuksen mukaisen tarkkuustestausratkaisun, joka tukee yksilöllistä adjuvanttihoitoa varhaisvaiheen ei-pienisoluisessa keuhkosyövässä (NSCLC).
Viitteet:
- Zer A, Ahn MJ, Barlesi F ym. Varhaisvaiheen ja paikallisesti edenneen ei-pienisoluisen keuhkosyövän hoito-ohjeet: ESMO:n kliinisen käytännön ohjeet diagnosointiin, hoitoon ja seurantaan. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Julkaisun aika: 06.05.2026

