Ihmisen EGFR-geenin 29 mutaatiot
Tuotteen nimi
HWTS-TM0012A-ihmisen EGFR-geenin 29 mutaatioiden havaitsemispakkaus (fluoresenssi-PCR)
Epidemiologia
Keuhkosyövästä on tullut maailmanlaajuisesti johtava syöpäkuolemien aiheuttaja, ja se uhkaa vakavasti ihmisten terveyttä. Ei-pienisoluinen keuhkosyöpä on syynä noin 80 prosenttiin keuhkosyöpäpotilaista. EGFR on tällä hetkellä tärkein molekyylikohde ei-pienisoluisen keuhkosyövän hoidossa. EGFR:n fosforylaatio voi edistää kasvainsolujen kasvua, erilaistumista, invaasiota, metastaasia, apoptoosin estämistä ja kasvaimen angiogeneesiä. EGFR-tyrosiinikinaasi-inhibiittorit (TKI) voivat estää EGFR-signalointireitin estämällä EGFR-autofosforylaatiota, mikä estää kasvainsolujen lisääntymistä ja erilaistumista, edistää kasvainsolujen apoptoosia, vähentää kasvaimen angiogeneesiä jne., jolloin saavutetaan kasvaimeen kohdennettu hoito. Lukuisat tutkimukset ovat osoittaneet, että EGFR-TKI:n terapeuttinen teho liittyy läheisesti EGFR-geenimutaation tilaan ja voi spesifisesti estää EGFR-geenimutaatiota sairastavien kasvainsolujen kasvua. EGFR-geeni sijaitsee kromosomin 7 (7p12) lyhyessä haarassa, sen koko pituus on 200 kb ja se koostuu 28 eksonista. Mutatoitunut alue sijaitsee pääasiassa eksoneissa 18–21, kodoneissa 746–753 eksonin 19 deleetiomutaatio muodostaa noin 45 % ja eksonin 21 L858R-mutaatio noin 40–45 %. NCCN:n ei-pienisoluisen keuhkosyövän diagnosointi- ja hoito-ohjeissa todetaan selvästi, että EGFR-geenimutaatiotestaus on tarpeen ennen EGFR-TKI:n antoa. Tätä testipakkausta käytetään epidermaalisen kasvutekijän reseptorin tyrosiinikinaasin estäjän (EGFR-TKI) lääkkeiden antamisen ohjaamiseen ja se tarjoaa perustan yksilölliselle lääketieteelle ei-pienisoluista keuhkosyöpää sairastaville potilaille. Tätä testipakkausta käytetään vain yleisten EGFR-geenin mutaatioiden havaitsemiseen ei-pienisoluista keuhkosyöpää sairastavilla potilailla. Testitulokset ovat vain kliinistä viitteenä, eikä niitä tule käyttää ainoana perustana potilaiden yksilölliselle hoidolle. Lääkäreiden tulee ottaa huomioon potilaan tila, lääkkeen käyttöaiheet ja hoito. Reaktiota ja muita laboratoriotestien indikaattoreita ja muita tekijöitä käytetään testitulosten kattavaan arviointiin.
Kanava
| FAM | IC-reaktiopuskuri, L858R-reaktiopuskuri, 19del-reaktiopuskuri, T790M-reaktiopuskuri, G719X-reaktiopuskuri, 3Ins20-reaktiopuskuri, L861Q-reaktiopuskuri, S768I-reaktiopuskuri |
Tekniset parametrit
| Säilytys | Neste: ≤-18 ℃ pimeässä; Kylmäkuivattu: ≤30 ℃ pimeässä |
| Säilyvyysaika | Nestemäinen: 9 kuukautta; Kylmäkuivattu: 12 kuukautta |
| Näytteen tyyppi | tuore kasvainkudos, jäädytetty patologinen leike, parafiiniin upotettu patologinen kudos tai leike, plasma tai seerumi |
| CV | <5,0 % |
| LoD | nukleiinihapporeaktioliuoksen havaitseminen 3 ng/μL villityypin taustalla, voi vakaasti havaita 1 %:n mutaatioasteen |
| Spesifisyys | Villityypin ihmisen genomisen DNA:n ja muiden mutanttityyppien kanssa ei ole ristireaktiivisuutta |
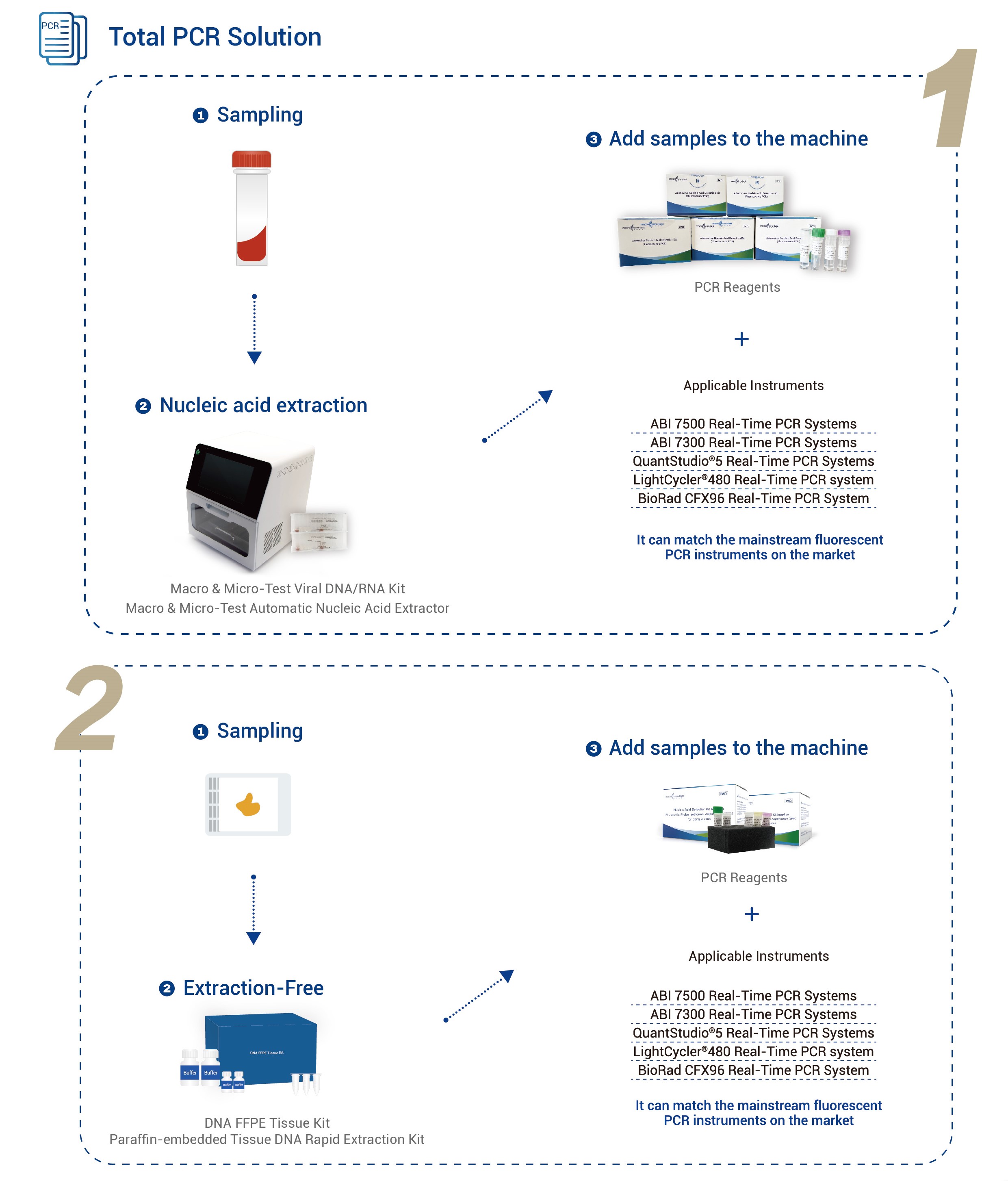
| Sovellettavat instrumentit | Applied Biosystems 7500 reaaliaikaiset PCR-järjestelmätApplied Biosystems 7300 reaaliaikaiset PCR-järjestelmät QuantStudio® 5 reaaliaikaiset PCR-järjestelmät LightCycler® 480 -reaaliaikainen PCR-järjestelmä BioRad CFX96 reaaliaikainen PCR-järjestelmä |